2022年7月16日,中国科学技术大学合肥微尺度物质科学国家研究中心、化学与材料科学学院的阳丽华课题组在国际学术期刊Nature Communications上发表了题为“Nanoparticle Elasticity Affects Systemic Circulation Lifetime by Modulating Adsorption of Apolipoprotein A-I in Corona Formation”的研究论文。该研究揭示了纳米颗粒的弹性如何影响其体内血液循环寿命、以及如何通过调控其蛋白冠从而实现这种影响,表明纳米颗粒弹性未来可望作为一个易于调节的参数用于合理利用蛋白冠。
纳米颗粒在疫苗、疾病诊疗等医学领域具有广阔应用前景。近期,研究发现纳米颗粒的弹性显著影响其细胞内吞效率与模式、血液循环寿命、和体内分布等生理命运。但是,颗粒弹性影响纳米颗粒生理命运的机制仍然未知。另一方面,纳米颗粒进入生命系统后,体液(如,血液)中的蛋白质会快速吸附到颗粒表面上并形成蛋白冠。决定纳米颗粒的体内生理身份的,正是其蛋白冠、而非其自身的尺寸、形状和表面化学等物化参数。为了合理利用蛋白冠、最终调控与改善纳米颗粒生理命运,需要理解纳米颗粒的弹性对其蛋白冠的影响。然而,此前还没有报告系统地研究过纳米颗粒弹性对蛋白冠的影响。
针对上述问题,阳丽华课题组制备了一系列大小、形状、表面化学相似但弹性在45 kPa–760 MPa可调的核壳纳米球(图1)作为模式纳米颗粒,从而成功将纳米颗粒弹性对其生理命运的影响与纳米颗粒大小、形状、表面化学等其他物化参数对其生理命运的影响分割开来独立研究,发现:(1)在实验小鼠模型中,纳米颗粒的弹性对其血液循环寿命的影响并非文献中普遍认为的“越软的颗粒血液循环寿命越长”那种单调性关系,而是具有非单调性、根据纳米颗粒弹性不同可分为三个不同区域、且弹性位于中间第二区域(15-75 kPa)的纳米颗粒具有最短血液循环寿命;(2)纳米颗粒的弹性与其细胞内吞效率之间缺乏明确关联。
同时,纳米颗粒与小鼠血浆混合后形成的蛋白冠,其组成也随纳米颗粒的弹性改变而发生非单调性变化。其中,载脂蛋白Apolipoprotein A-I(ApoA1)是唯一一种能在至少一个纳米颗粒表面蛋白冠中达到相对丰度>20%的蛋白质、同时也是蛋白冠中相对丰度与纳米颗粒血液清除寿命具有强烈相关性的唯一一种蛋白质,显示纳米颗粒的弹性通过调控蛋白冠中ApoA1的吸附从而影响纳米颗粒的血液循环寿命。值得一提的是,当上述纳米颗粒的表面由聚乙二醇化(PEGylated)脂质双分子层外壳变为不含聚乙二醇(PEG-free)的天然磷脂双分子层后,所得纳米颗粒表现出了类似的“弹性-蛋白冠组成”变化趋势。
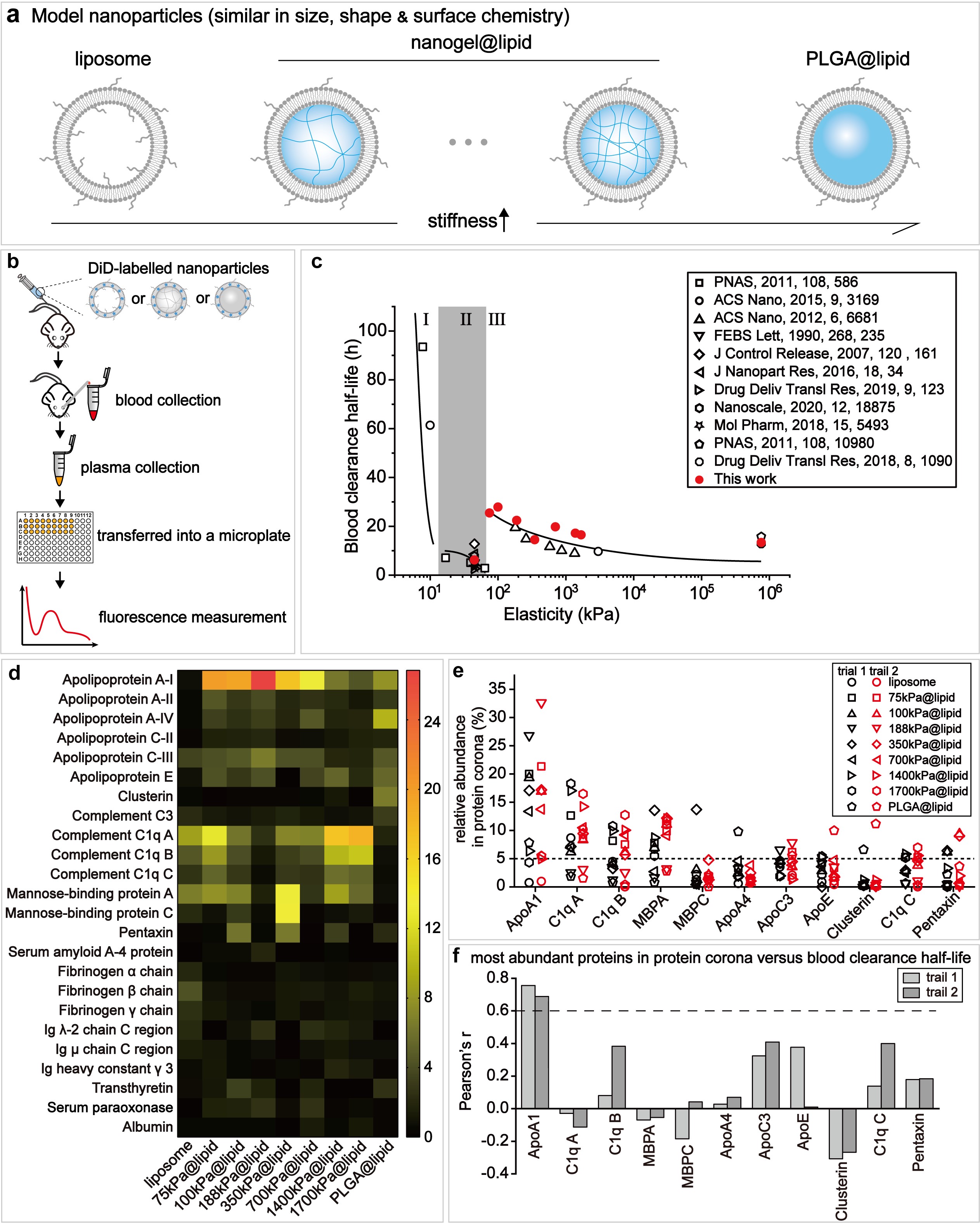
图1. a大小、形状和表面化学等相同但弹性不同的模式纳米颗粒。b获取纳米颗粒血液滞留曲线的血液循环测试示意图。c纳米颗粒的血液清除半衰期与纳米颗粒弹性的关系曲线。d不同弹性纳米颗粒的蛋白冠中蛋白质相对丰度热图。e至少在一个纳米颗粒的蛋白冠中相对丰度大于5%的蛋白在不同颗粒蛋白冠中的相对丰度分布。h蛋白在不同颗粒蛋白冠中相对含量与颗粒血液清除半衰期的相关性系数Pearson’s r。
该研究项目得到了国家自然科学基金委、教育部和安徽省自然科学基金的资助。该论文的第一作者为中国科学技术大学化学与材料科学学院博士生李明洋,通讯作者为中国科学技术大学阳丽华副教授。
原文链接:https://doi.org/10.1038/s41467-022-31882-4
(化学与材料科学学院、合肥微尺度物质科学国家研究中心、科研部)



